| Главная » Статьи » Урочно-внеурочная деятельность » 9 Класс |
Презентация к уроку по теме Белки Цель: развитие и систематизация на межпредметном уровне знаний о природных высокомолекулярных веществах – белках, их строении, свойствах и значении в жизни человека. Задачи урока:
Тип урока: урок изучения и первичного закрепления новых знаний. Оборудование: мультимедийная презентация, единая коллекция цифровых образовательных ресурсов по химии 10 класс по теме « Белки». Реактивы для демонстрационного эксперимента: растворы куриного белка, NaCl (насыщ. раствор), CuSO4, NaOH, HNO3 (конц.), сок картофеля, вареный картофель, перекись водорода, вода, нагревательный прибор, зажим, спички. ХОД УРОКА I. Организационный момент II. Актуализация знаний Мы изучили соединения, имеющие большое значение в жизни живых организмов. Теперь переходим к веществам, имеющим первостепенное значение. Тема урока: «Белки» Учитель: Что такое жизнь? Откуда она взялась на Земле? Эти вопросы волнуют людей всегда. В течение веков копились наблюдения, проводились исследования, создавались теории. Одни служили основой новых исследований, другие гибли ввиду несостоятельности… Белки – русское название данного класса, международное – протеины. Эти названия – синонимы. Названия этого класса веществ подтверждают их первостепенное значение. Затем интерактивный тест на биологические функции белков (ЦОР, карточка ресурса № 125523). Биологические функции белков Задание на листочке – историческая справка (сформулировать в 1-2 предложениях роль ученых в изучении белков, соблюдая хронологический порядок). III. Изучение новой темы А знаете ли Вы: 1. Белок никогда не переходит в жир – совет врача-диетолога. Понять, каким образом белки осуществляют перечисленные выше многообразные функции, непросто. Единственный способ приблизиться к решению этой задачи – узнать, из чего построен белок, как расположены структурные элементы, составляющие его молекулу, по отношению друг к другу и в пространстве, как они взаимодействуют друг с другом и веществами внешней среды, т.е. изучить строение и свойства белков (ЦОР – структуры белков: карточки ресурсов № 125484, 125485, 125489,125492). Вывод: раскрыли причинно-следственную зависимость: функции – строение. Белки – полимеры, мономеры – альфа-АК. – Назовите известные Вам белки, укажите их местонахождение? Ответ:
Историческая справка Начало их изучения положено в середине 18 в. итальянцем Я. Беккари, но только через 100 лет ученым удалось систематизировать свойства белков и сделать вывод, что белки – это главный компонент живых организмов. Компьютерные изображения структуры белков Вопросы для обсуждения: Примеры источников белка? (Их источниками являются мясо, рыба, молоко, соя, бобы, горох.) Вывод: Белки встречаются в растительных и животных организмах. – Какие элементы входят в состав белков? Среднее содержание химических элементов в белках: (слайд 6) С (углерод) – 50-55%; О (кислород) – 19-24%; N (азот) – 15-18%; Н (водород) – 6-8 %; S (сера) – 0,3-2,5%; Р (фосфор) – до 0-5%. В состав белков могут входить хлор, фтор, йод, а также металлы: цинк, магний, железо, медь. – Какова средняя масса белковых молекул? Огромна.
Вывод: Ни одно из природных соединений не обладает такими безграничными потенциальными возможностями изомерии, как белки. Именно так реализуется в природе бесконечное разнообразие структуры белковых тел, дающее начало миллионам растительных и животных видов. Каждый вид обладает собственными видами белков. Если бы в первичной структуре белка не было бы заложено этого качества, то не было бы такого разнообразия жизненных форм, к которым относимся и мы . – Какая структура является самой прочной? Почему? (Первичная, т.к. связи прочные, ковалентные.) IV. Ученические эксперименты Исследуем свойства белков с соблюдением правил ТБ 1. Доказательство наличие белка только в живых организмах. В 3 пробирки – свежевыжатый сок картофеля, кусочки сырого картофеля, вареный картофель . К ним добавили перекись водорода. Делаем вывод. Оборудование и реактивы: альбумин, нагревательный прибор, конц. азотная кислота, гидроксид натрия, сульфат меди (II), раствор поваренной соли, вода, набор пробирок. Это интересно: Зачем маринуют мясо? Под воздействием уксусной кислоты или лимонной происходит частичный гидролиз белков. Белки распадаются на поли – и дипептиды. В желудке под влиянием ферментов этот процесс продолжается и в итоге приводит к образованию аминокислот. Таким образом, маринование облегчает переваривание белка.
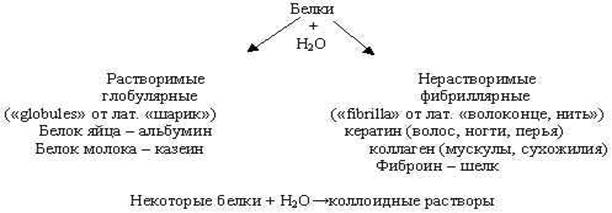
2. Отношение к воде образуют коллоидные растворы (слайд 9) Альбумин + вода; желатин + вода, прорастание семян фасоли, гороха и т.д.
Это интересно: В чем причина образования пены на поверхности мясных бульонов, жареных, рыбных, и мясных изделий? (слайд 10) (Объясняется свертыванием растворимых в воде белков (альбумины, глобумины). 3. Осаждение белков может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном — третичная, а затем — вторичная, и белок остается в виде полипептидной цепи. Этот процесс частично обратим: если не разрушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенности строения макромолекулы белка определяются его первичной структурой – обратимое (высаливание):
Необратимое – денатурация (стр. учебника 160). – Какой реакцией можно доказать наличие в белках углерода, водорода, кислорода? (Реакцией разложения при температуре яичного белка. При этом образуются летучие продукты – запах жженых перьев. Эта особенность белков используется для их обнаружения. Разрушаются все структуры белка.) Вывод: Денатурация белков – потеря естественных свойств (растворимости и др.) вследствие нарушения структуры молекул. 4. Цветные (качественные) реакции на белок: Ксантопротеиновая реакция: желтое окрашивание– (обнаружение бензольных ядер в аминокислотных остатках). Поместите кусочек прессованного творога в пробирку и добавьте несколько капель азотной кислоты. Осторожно нагрейте. (Дают не все белки).
Биуретовая реакция: фиолетовое окрашивание – (распознавание пептидных связей). Налейте в пробирку 2 мл яичного белка. Добавьте такой же объем концентрированного раствора гидроксида натрия и несколько капель раствора медного купороса.
Биологическое значение белков Белки входят в состав мозга, всех внутренних органов, скелета и суставов, кожи, волосяного покрова и т. д. В крови в растворенном виде содержится белок гемоглобин, обеспечивающий перенос кислорода по всему организму. Многие белки выполняют роль ферментов – катализаторов обмена веществ в живых организмах. В растениях белки концентрируются в основном в семенах. Белковый обмен тесно взаимосвязан с обменом углеводов и нуклеиновых кислот. Существенное влияние на белковый обмен оказывает характер питания, качественный и количественный белковый состав пищи. Источниками белков могут служить не только животные продукты (мясо, рыба, яйца, творог), но и растительные, например, плоды бобовых (фасоль, горох, соя, арахис, которые содержат до 22-23 % белков по массе), орехи и грибы. Однако больше всего белка в сыре (до 25 %), мясных продуктах (в свинине 8-15 %, баранине 16-17 %, говядине 16-20 %), в птице (21 %), рыбе (13-21 %), яйцах (13 %), твороге (14 %). Молоко содержит 3 % белков, а хлеб 7-8 %. Среди круп чемпион по белкам – гречневая (13 % белков в сухой крупе), поэтому именно ее рекомендуют для диетического питания. Чтобы избежать «излишеств» и в то же время обеспечить нормальную жизнедеятельность организма, надо, прежде всего, дать человеку с пищей полноценный по ассортименту набор белков. Если белков в питании недостает, взрослый человек ощущает упадок сил, у него снижается работоспособность, его организм хуже сопротивляется инфекции и простуде. Что касается детей, то они при неполноценном белковом питании сильно отстают в развитии: дети растут, а белки – основной «строительный материал» природы. Каждая клетка живого организма содержит белки. Мышцы, кожа, волосы, ногти человека состоят главным образом из белков. Более того, белки – основа жизни, они участвуют в обмене веществ и обеспечивают размножение живых организмов. Присутствие протеинов в кремах против морщин, тониках, пене для ванны и др. оберегает кожу от высушивания, придает ей мягкость и упругость. Применяются протеины также в косметических средствах для ногтей. Являются активными веществами в средствах ухода за волосами (лечебные бальзамы, кондиционеры для волос). Благотворно действуют на нарушенную структуру волос, укрепляют их корни. V. Вопросы для самоконтроля и интерактивный тест (ЦОР, карточка ресурса № 125493)
VI. Творческое задание (парная работа) (слайды 11-16) Составить синквейн по теме «Белки» 1. Белки. VII. Итог урока Выставить оценки за урок. Поблагодарить учеников (слайд 17) VIII. Домашнее задание: параграф 38, записи по тетради выучить. Использованная литература: 1. Г.Е.Рудзитис, Ф.Г. Фельдман «Химия 10», Москва, Просвещение, 2010/
| |
| Просмотров: 781 | |
| Всего комментариев: 0 | |